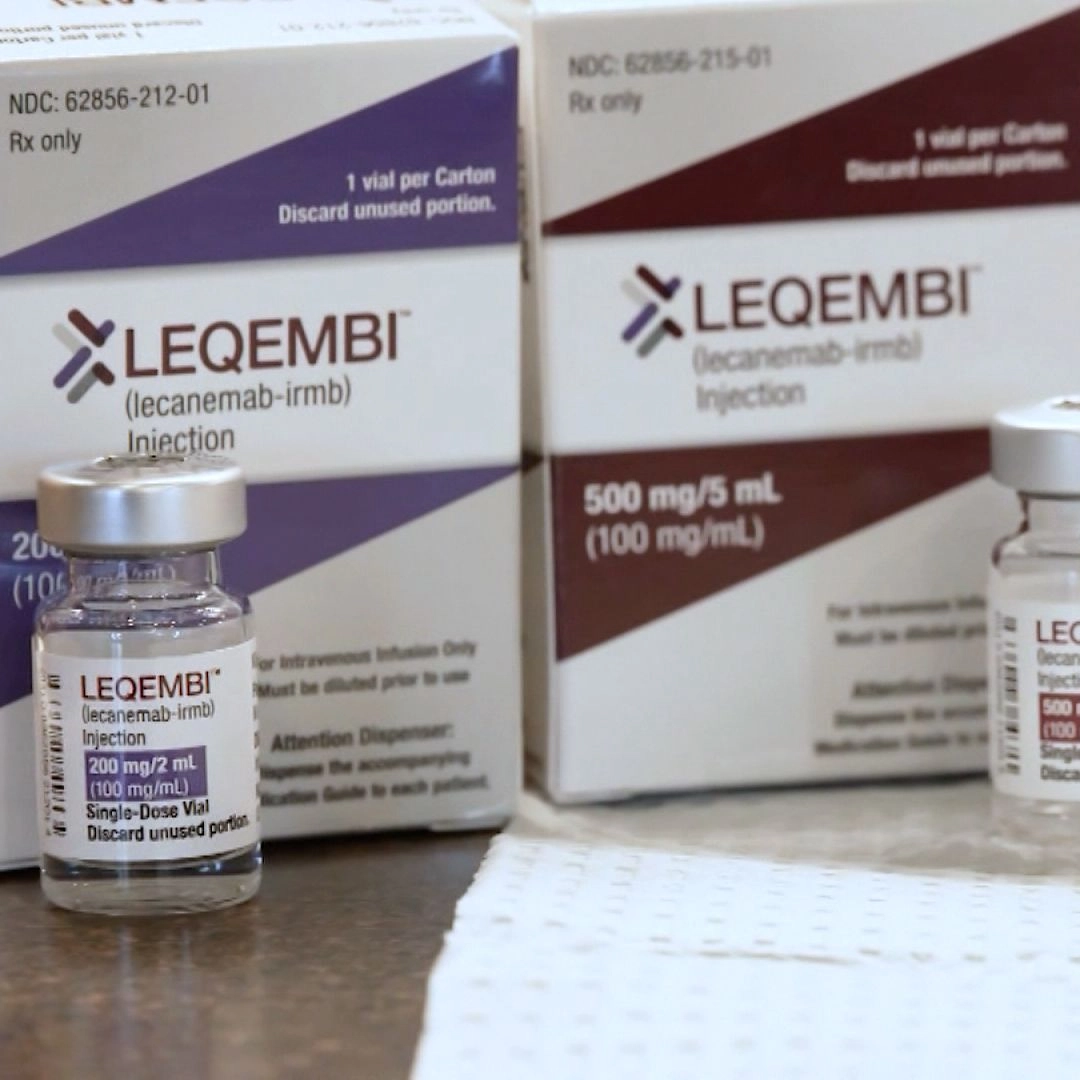
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso do lecanemabe para o tratamento da doença de Alzheimer no Brasil. Inédito no país, o medicamento é um anticorpo monoclonal da classe dos produtos biológicos e passa a integrar o rol de terapias autorizadas para a fase inicial da doença.
Segundo o registro aprovado, o lecanemabe é indicado para pacientes adultos com comprometimento cognitivo leve ou demência leve decorrentes do Alzheimer, desde que a patologia amiloide esteja confirmada. O uso é restrito a pacientes que não sejam portadores ou sejam heterozigotos do alelo ε4 da apolipoproteína E (ApoE ε4), fator genético associado a maior risco de efeitos adversos.
O tratamento deve ser feito por infusão intravenosa, com duração aproximada de uma hora, administrada a cada duas semanas.
Com a decisão da Anvisa, o medicamento está oficialmente autorizado para distribuição e uso no Brasil. A data de início da comercialização, no entanto, ainda depende do laboratório responsável pelo registro, que definirá prazos, logística e preço.
O lecanemabe atua na redução das placas beta-amiloides no cérebro, associadas ao desenvolvimento do Alzheimer, e representa um avanço terapêutico para pacientes diagnosticados precocemente, embora não seja considerado uma cura para a doença.